Comprendre la dynamique du sodium au niveau microscopique
Les batteries à base d’ions de lithium sont très performantes et fournissent de l’énergie aux ordinateurs portables, aux téléphones mobiles et, de plus en plus, aux voitures électriques. Mais l’utilisation du lithium a des inconvénients : c’est un élément coûteux, dont l’extraction a un impact environnemental. Une possibilité pour contourner ces inconvénients consisterait à utiliser du sodium à la place du lithium. Le sodium présente en effet des propriétés chimiques analogues au lithium, tout en étant disponible en quantités nettement plus importantes. Lors de la charge et de la décharge d’une batterie à base de lithium, les ions de cet element se déplacent – dans l’électrode et hors de l’électrode. Pour construire une batterie à base d’ions de sodium, il faut donc comprendre comment le sodium se déplace dans les matériaux concernés. Des chercheurs de l’Institut Paul Scherrer ont à présent préparé ainsi que déterminé, pour la première fois, les chemins qu’empruntent les ions de sodium dans un matériau susceptible d’être utilisé dans une batterie. Concrètement, ils ont analysé le composé Na0,7CoO2 au moyen de la diffusion neutronique à la source de neutrons suisse SINQ du PSI. Il s’est avéré que ces chemins se modifient avec la température, et que ces modifications dépendent directement de petits changements de la structure atomique du matériau. Ces connaissances permettent maintenant de réfléchir au moyen de créer de nouveaux matériaux présentant des propriétés nécessaires aux futures batteries, grâce à une légère modification de la structure ou de la composition. Les chercheurs ont publié leurs résultats dans la revue spécialisée Physical Review Letters.
La question de la transformation et du stockage efficace de l’énergie est l’un des problèmes scientifiques majeurs auquel notre société fait face. Dans les téléphones mobiles, les ordinateurs portables et, de plus en plus, dans les voitures électriques, ce stockage d’énergie est normalement assuré par des batteries à base d’ions de lithium. Les batteries connaissent aussi un essor important dans un autre domaine : le stockage d’énergie local, directement sur les sites des parcs éoliens ou des centrales solaires. Mais l’utilisation de batteries à base de lithium présente aussi des inconvénients. Ces dernières sont en effet relativement coûteuses, et l’extraction du lithium a un impact sur l’environnement car cet élément est relativement rare sur la Terre (20 ppm), et chimiquement très réactif.
Le sodium comme alternative au lithium dans les batteries
Une possibilité pour contourner ces inconvénients serait de remplacer le lithium (Li) du matériau des électrodes dans les batteries rechargeables par du sodium (Na). Le sodium présente en effet des propriétés chimiques similaires au lithium, mais il est 1000 fois plus abondant, aussi bien dans le sol (26'000 ppm) que dans l’eau de mer, en tant que composant du sel de cuisine dissous (NaCl) (15'000 ppm). Les batteries à base de sodium seraient donc en principe plus écologiques, plus faciles à recycler et jusqu’à cinq fois moins chers. Cependant, comme les ions de sodium sont plus gros et plus lourds que les ions de lithium, la tension nominale d’une batterie au sodium serait un peu plus basse. On s’attend donc à ce que les batteries à base de sodium aient d’abord une plus faible densité énergétique que les actuelles batteries à base de lithium. Notons tout de fois que ce dernier point n’est pas un inconvénient pour des applications stationnaires, telles que celles en combinaison avec de eoliennes ou des centrales solaires.
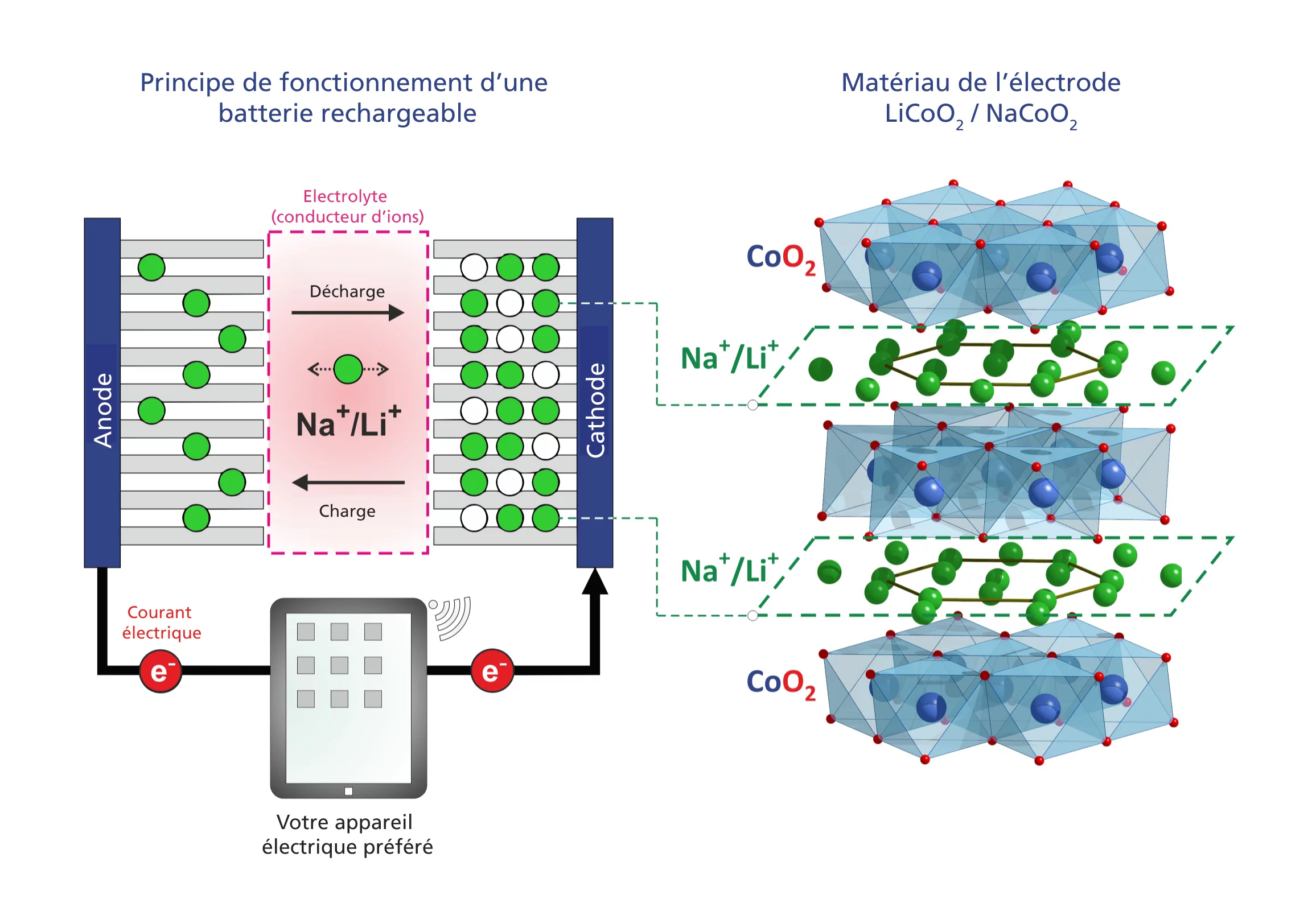
Dans les deux types de batteries, lors de la charge et de la décharge, les ions se deplacent entre les deux électrodes ; de l’une à l’autre, un électrolyte faisant office de pont pour le transport des ions. Afin de pouvoir développer de nouvelles batteries, il faut analyser le comportement des matériaux correspondants et comprendre au niveau atomique comment les ions s’y déplacent. En collaboration avec leurs collègues de l’EPF Zurich, - du laboratoire de recherche Toyota, et du Centre de recherche - CROSS au Japon, des chercheurs de l’Institut Paul Scherrer ont prepare et analysé le matériau Na0,7CoO2. Au niveau de la structure, ce dernier ressemble aux matériaux couramment utilisés pour les cathodes des batteries à base de lithium mais elle contient du sodium à la place du lithium. Elle présente une structure stratifiée, où des couches d’oxyde de cobalt alternent avec des couches d’ions de sodium.
De petites modifications de la structure entraînent d’importantes modifications au niveau de la dynamique
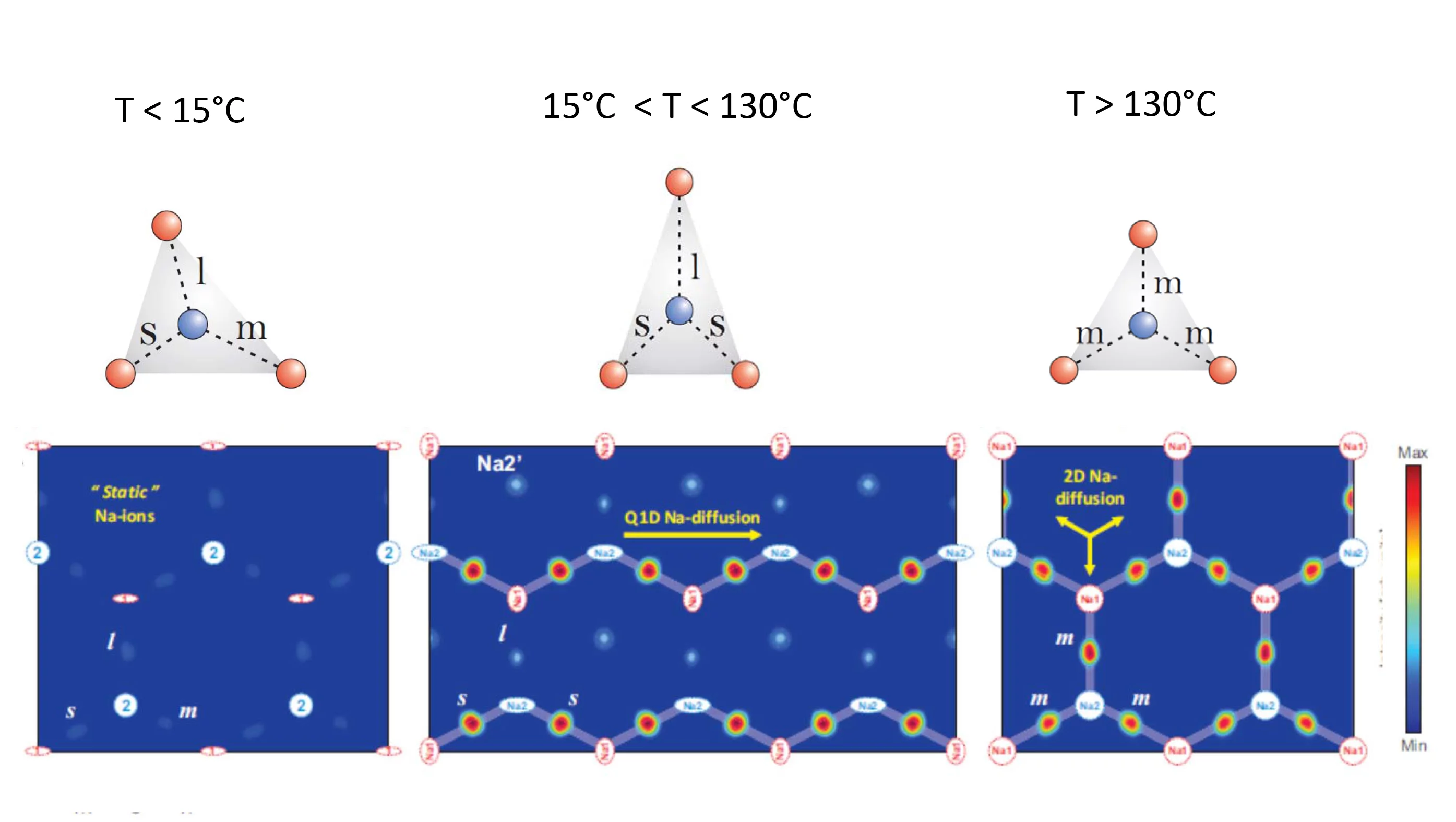
La plupart des analyses de la conductivité électrique par les ions ne fournissent que des informations approximatives sur la vitesse à laquelle les ions se déplacent. En revanche, la technique la diffusion neutronique utilisée par les chercheurs au PSI montre en détail les chemins empruntés par les ions à échelle atomique. Les expériences ont montré que le déplacement des ions dépendait clairement de la température. A des températures inférieures à 15°C, les ions de sodium peuvent à peine bouger, explique Marisa Medarde, chercheuse au PSI spécialisée dans le domaine des matériaux, et premier auteur de la publication. Entre 15°C et 130°C, ils ne se déplacent que dans une seule dimension, en suivant des chemins bien définis, alors qu’à des températures plus élevées ils peuvent se déplacer librement dans toute la couche de sodium. Les modifications qui interviennent au niveau de la dynamique sont liées à une légère distorsion de la structure du matériau : à des températures supérieures à 130°C, les positions des ions de sodium dans les couches forment un arrangement triangulaire. Les côtés de ces triangles sont tous de longueur identique, de sorte que l’énergie dont un ion a besoin pour sauter d’un sommet au suivant est toujours la même, indépendamment de la direction dans laquelle il se déplace. Dès que la température est inférieure à 130°C, l’énergie thermique des ions ne suffit plus pour ce mouvement. C’est alors qu’il se produit un minuscule changement dans l’arrangement des positions préférées du sodium : un côté du triangle se raccourcit. Sauter entre des sommets séparés par une distance plus courte coûte moins d’énergie, de sorte que ce raccourcissement rend possible le mouvement des ions de sodium à des températures inattendument basses.
Contrôler le mouvement des ions dans les matériaux de l’accumulateur
Grâce à ces résultats, nous avons une toute nouvelle compréhension de la complexité de la dynamique de ces liaisons, explique Martin Månsson, spécialiste au PSI du stockage d’énergie et des sciences des matériaux. Ils montrent également à quel point des effets de faible ampleur suffisent à créer des conditions optimales pour le déplacement des ions. Cet acquis nous permet de déterminer comment optimiser et contrôler le transport des ions dans les matériaux des batteries. Par exemple, en remplaçant dans les matériaux actuels un élément chimique par un autre, en exposant le matériau à une pression extérieure, ou en développant des composés complètement nouveaux , en concevant leur structure atomique de manière ciblée.
Des neutrons pour analyser les matériaux
Pour leurs analyses, les chercheurs ont utilisé la source de neutrons suisse SINQ au PSI. Dans cette expérience, un faisceau de neutrons traverse un échantillon du matériau analysé, et certains de ces neutrons interagissent avec l’échantillon, ce qui leur fait modifier leur trajectoire : les experts parlent alors de diffusion neutronique. Le nombre de neutrons déviés dans une direction quelconque contient des informations sur la structure interne du matériau. Pour certaines directions on observe des maximas nets (pics ) au niveau du nombre de neutrons déviés, ce qui reflète l’existence d’un arrangement régulier des atomes et des ions dans le matériau. Dans le cas analysé ici, l’un de ces pics est nettement divisé en deux quand la température decend en dessous de 130°C,. Cela indique que les distances entre les positions du sodium ne sont plus toutes équivalentes et qu’elles correspondent à un triangle légèrement déformé. Ces légères distorsions sont apparemment la clé pour la conception des materiaux avec des mechanismes de transport des ions à la carte
, souligne Martin Månsson.
Texte: Paul Piwnicki
À propos du PSI
L’Institut Paul Scherrer développe, construit et exploite de grandes installations de recherche complexes et les met à disposition de la communauté nationale et internationale. Les principales recherches de l’Institut sont centrées dans le domaine matière et matériaux, energie et environnement, santé. Avec 1500 collaborateurs et un budget annuel d’environ 300 millions CHF, le PSI est le plus grand centre de recherche de Suisse.
Contact
Marisa Medarde, Laboratoire de développement et méthodes (LDM), Institut Paul Scherrer,5232 Villigen PSI, Suisse
Téléphone : +41 56 310 3283 ; e-mail : marisa.medarde@psi.ch
Martin Månsson, Laboratoire de diffusion neutronique (LNS), Institut Paul Scherrer, 5232 Villigen PSI, et
Laboratoire de magnétisme quantique (LQM), École polytechnique fédérale de Lausanne (EPFL), 1015 Lausanne, Suisse ;
Téléphone : +41 56 310 5534 ; e-mail: martin.mansson@psi.ch
Publication originale
1D to 2D Na+ Ion Diffusion Inherently Linked to Structural Transitions in Na0.7CoO2M. Medarde, M. Mena, J. L. Gavilano, E. Pomjakushina, J. Sugiyama, K. Kamazawa, V. Yu. Pomjakushin, D. Sheptyakov, B. Batlogg, H. R. Ott, M. Månsson, and F. Juranyi
Phys. Rev. Lett. 110, 266401 (2013),
DOI: 10.1103/PhysRevLett.110.266401